¿Estás buscando información sobre el volumen de un gas en condiciones normales? Entonces has llegado al lugar correcto. En este artículo te explicaremos todo lo que necesitas saber sobre este tema.
¿Qué son las condiciones normales?
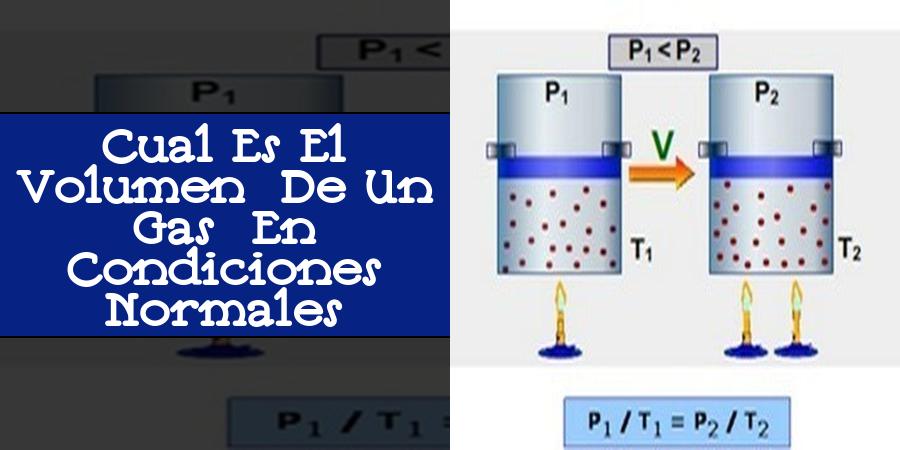
Antes de hablar sobre el volumen de un gas en condiciones normales, es importante entender qué son las condiciones normales. Las condiciones normales se refieren a una temperatura de 0 grados Celsius y una presión de 1 atmósfera.
¿Cómo se calcula el volumen de un gas en condiciones normales?

Para calcular el volumen de un gas en condiciones normales, se utiliza la ecuación de estado de los gases ideales, que es la siguiente:
V = nRT/P
Donde:
- n = número de moles del gas
- R = constante universal de los gases ideales (0,0821 L·atm/K·mol)
- T = temperatura en Kelvin
- P = presión en atmósferas
Para calcular el volumen de un gas en condiciones normales, se deben tener en cuenta los siguientes valores:
- n = 1 mol
- R = 0,0821 L·atm/K·mol
- T = 273,15 K (0 grados Celsius en Kelvin)
- P = 1 atm
Reemplazando estos valores en la ecuación, obtenemos:
V = (1 mol)(0,0821 L·atm/K·mol)(273,15 K)/(1 atm) = 22,4 L/mol
Por lo tanto, el volumen de un gas en condiciones normales es de 22,4 litros por mol.
¿Por qué es importante conocer el volumen de un gas en condiciones normales?
Conocer el volumen de un gas en condiciones normales es importante en varias áreas de la ciencia, como la química y la física. Por ejemplo, en la química se utiliza para calcular la cantidad de gas que se necesita para una reacción química determinada. En la física, se utiliza para calcular la densidad de un gas en condiciones normales.
Conclusiones

el volumen de un gas en condiciones normales es de 22,4 litros por mol. Conocer este valor es importante en diversas áreas de la ciencia, y se calcula utilizando la ecuación de estado de los gases ideales. Esperamos que esta información te haya sido útil.